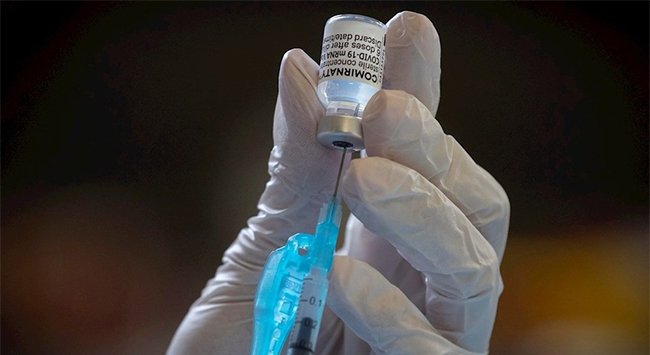
En las pruebas, agregan, la vacuna fue 'bien tolerada en términos generales'.
Por: EFEÂ
La Haya.-  La Agencia Europea de Medicamentos (EMA) respaldó este viernes la extensión del uso de la vacuna anticovid de Pfizer/BioNTech a los adolescentes de entre 12 y 15 aí±os, lo que la convierte en el primer preparado contra Covid-19 con respaldo científico en la Unión Europea para los menores de 16 aí±os.
En una rueda de prensa, Marco Cavaleri, jefe de Estrategia de Vacunas, confirmó esta âindicación pediátricaâ acordada hoy en una reunión extraordinaria del comité de fármacos de uso humano (CHMP), que ha concluido que la vacuna es âseguraâ y eficaz en nií±os de esa edad.
Pfizer y BioNTech probaron en fase 3 su vacuna contra el Covid-19 en 2 mil 260 adolescentes y aseguraron que su efectividad fue del 100 por ciento y con una âsólidaâ respuesta inmunológica.
En las pruebas, agregan, la vacuna fue âbien tolerada en términos generalesâ.
La vacuna, que ya está aprobada en la Unión Europea desde diciembre para mayores de 16 aí±os, tendrá la misma aplicación en nií±os de 12 a 15 aí±os que el que se le está dando en la actualidad a los adultos: se administrará en dos inyecciones en los músculos de la parte superior del brazo, con âtres semanasâ de diferencia entre la primera y la segunda dosis.
Por otro lado, la EMA aseguró que mantiene su recomendación de inyectar una segunda dosis de la vacuna de AstraZeneca a quienes recibieron una primera sin mostrar efectos adversos de coagulación sanguínea porque no hay evidencias de que la segunda inyección aumente el riesgo de desarrollar trombocitopenia con respecto a la primera dosis.
El regulador europeo subrayó que hay evidencias ofrecidas por algunos estudios, que aún deben ser analizados por la EMA, sobre la efectividad del uso de una segunda dosis de una vacuna de ARNm, cuyo resultado muestra que âno hay preocupación desde una perspectiva de seguridadâ y que este es âun enfoque realmente eficazâ desde el punto de vista inmunológico.